首頁
案例實績
特用化學與製藥
無菌過濾就等於沒有內毒素風險嗎?
2026-03-16
無菌過濾就等於沒有內毒素風險嗎?

在製藥製程中,0.2 um 濾心常被用作無菌過濾用來去除細菌與顆粒雜質。
是否就等於產品的潔淨度已得到確保呢?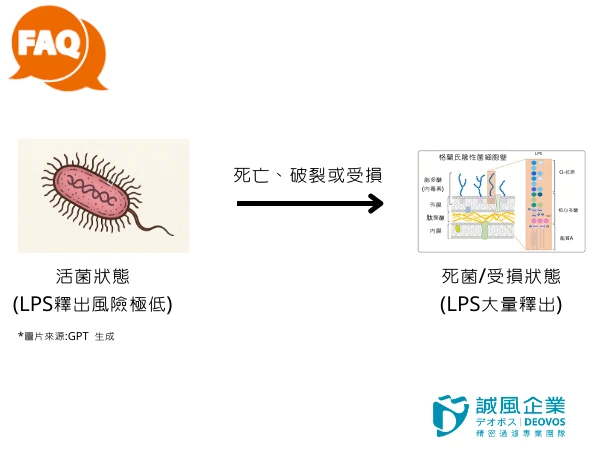
先前提過內毒素是在何種狀況才會出現?
當這些細菌在生長、裂解 (lysis)、死亡或細胞壁自然脫落時,內毒素就會釋放到環境中(如水、培養基、藥液)。
因此當產品經過0.2um濾心過濾後,我們可以確定的是產品是無菌狀態。
而內毒素不是完整細菌,只是存在於細胞壁上的其中一小部分,因此無法依靠孔徑截留(如 0.2 μm 濾心)有效去除。
故需要透過製程管控(控制內毒素的來源)以及具有吸附效果的濾心產品將產品殘留的內毒素降至最低。
通常可以分為內部驗證跟委外確校
在前期實驗室階段進行條件設定,製程手法,配方調整等初期lab試驗
由於有時間跟成本效益考量
多數都會搭配市售快速檢驗套組內部驗證進行條件等篩選
*內部驗證多作為自主品管/開發 使用,無法作為稽核或者送審用的文件

當產品生產條件定案之後會進行多次的小型量產試驗
這時候就會搭配外部經過TAF/TFDA認證的實驗室進行內毒素分析試驗
檢測費用以及檢測方式等都可以直接在衛福部公告資訊找到相關
當產品進到這個階段時,基本上原料,生產流程,製程手法使用耗材等都算是定案不會異動
誠風這邊也遇過從開發階段都是直接委外檢測的客戶
如何靈活使用內部資源或委託外部驗證,就取決於各公司政策方向
誠風企業常常有一句話[沒有最好的濾心,只有最適合的濾心]
誠風企業團隊可以依照您的產品或者預算需求提供最適合的方式
歡迎與誠風精密過濾專業團隊討論各式需求
